پیوند فلزی
در این مقاله قصد داریم در مورد فلزات و خواص آن صحبت کنیم. تعریف پیوند فلزی را بیاموزیم و ویژگیهای پیوندهای فلزی از جمله استحکام پیوند فلزی را درک کنیم. مطالب این مقاله باعث میشود تا درک درستی از خواص فلزات مانند هادی بودن (انتقال الکتریسیته و گرما)، چکش خواری و شکل پذیری، استحکام و … بدست آوریم.

تعاریف
اگر در مورد پیوند کووالانسی و یونی اطلاع داشته باشید، میدانید که این پیوندها میان دو اتم ایجاد میشوند. هنگامی که دو اتم الکترونهایشان را به اشتراک میگذارند، یک پیوند کووالانسی تشکیل میدهند. زمانیکی که یک اتم، الکترون را از دیگری جدا میکند و یونهای مثبت و منفی حاصله به یکدیگر جذب میشوند، در واقع آن اتمها یک پیوند یونی تشکیل دادهاند.
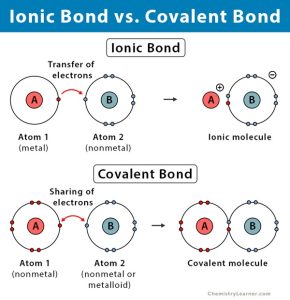
شکل 1: پیوند یونی و پیوند کووالانسی
پیوند فلزی با پیوندهای کووالانسی و یونی داری تفاوت زیادی است، اما هدف یکی است: دستیابی به حالت انرژی پایینتر. در پیوند فلزی به جای پیوند بین دو اتم، الکترونها بین بسیاری از اتمهای یک عنصر فلزی به اشتراک گذاشته میشوند.
نگاهی به اطراف خود بیاندازید و قطعهای فلزی بیابید. این قطعه کوچک فلز، همانند استخری که پر از آب است، دارای مخزن بزرگی از الکترونهای ظرفیت است که به عنوان دریایی از الکترونها آزاد یا الکترونهای غیرمحلی شناخته میشوند.
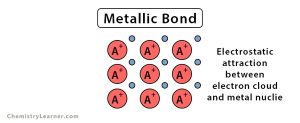
شکل 2: پیوند فلزی
برای درک بهتر پیوند فلزی، تصور کنید وان حمام خود را از پایین تا بالا به طور کامل با گویهای صلب فلزی پر کردهاید. این گویها وقتی که فضای وان را پر میکنند، آرایش منظمی به خود میگیرند. آیا فاصلهای بین گویها میبینید؟ حالا اگر شیر آب را باز کنید و درب لوله تخلیه آب (فاضلاب) را ببندید، آب آن فضاها را پر میکند. چیزی که اکنون مشاهده میکنید، چیزی شبیه پیوند فلزی است. در واقع این گویها، اتمهای فلزی هستند و آب نشاندهنده الکترونهای ظرفیتی است که بین همه اتمها مشترک است.

شکل 3: گویهای صلب فلزی در کنار هم با آرایش منظم
زمانیکه الکترونهای لایه ظرفیت از اتم اصلی خود جدا میشوند و در فضا به حالت شناور در میآیند، این اتمها به یونهای مثبت تبدیل میشوند. در نتیجه این عمل، ساختار منظمی از اتمهای فلزی مثبت به وجود میآید که توسط دریایی از الکترونهای منفی احاطه شده است و یونها را مانند چسب در کنار هم نگه میدارد.
به زبان ساده، پیوند فلزی روشی است که اتمهای فلز در یک ماده فلزی در کنار هم قرار میگیرند. پیوند فلزی نوعی پیوند شیمیایی شبیه پیوند کووالانسی است. اتمهای فلزات توسط نیروهای ناشی از الکترونهای ظرفیت کنار هم نگه داشته میشوند. منظور از الکترون ظرفیت، الکترونی است که در دورترین یا خارجترین سطح انرژی یک اتم یافت میشود. به دلیل ماهیت اتمهای فلز، الکترونهای ظرفیت پیوند محکمی با هسته اتم ندارند. این خاصیت، به الکترونهای ظرفیت اجازه میدهد تا مکانیابی شوند یا بتوانند از اتم اصلی دور شوند. فلزات دارای اتمهای نزدیک به هم هستند. همانطور که این الکترونهای ظرفیت از اتمهای اصلی خود جدا می شوند، از یک هسته به هسته دیگر حرکت میکنند. این کار، یک نوع ابر از الکترون های جدا شده یا سرگردان در فلز را تشکیل میدهد. از آنجایی که الکترونها، هستههای اتم اصلی را ترک کردهاند، در آن هستهها پروتونهای بیشتری نسبت به مقدار الکترونهای اتم باقی میماند. این عمل، باعث میشود اتم ها یونهایی با بار مثبت داشته باشند. نیروهای بین هستههای مثبت و ابر الکترونهای ظرفیت نیروی منسجمی ایجاد میکند که اتمهای فلز را به روشی منحصربهفرد در کنار هم نگه میدارد که باعث میشود فلز، خاصیت فلزی داشته باشد. طبق تعریف پیوند فلزی، این پیوند شیمیایی فقط در مواد فلزی وجود دارد.
پیوند فلزی چگونه تشکیل میشود؟
برای توصیف فرآیند تشکیل پیوند فلزی، از مفهوم دریا یا ابر الکترونها برای کمک به تجسم مکانیابی الکترونها استفاده شده است. الکترونهای ظرفیت فلزات، تنها با هستههای خود پیوند سست دارند، زیرا توسط سطوح انرژی داخلی بیشتر توسط الکترونها احاطه شدهاند. به عبارت دیگر، الکترونهای ظرفیت در یک پیوند فلزی میتوانند با هر اتمی در نمونه فلزی مرتبط شوند. این وضعیت، همراه با آرایش شبکهای و دارای الگوی نزدیک به اتمها، به الکترونهای لایه ظرفیت اجازه میدهد تا از یک اتم والد خاص و هسته مرتبط با آن، به صورت آزادانه پرسه بزنند. این دریا یا ابر الکترونها دارای بار جمعی منفی هستند و به صورت الکتریکی به سمت هستههای دارای بار مثبت جذب میشوند و در نتیجه یک پیوستگی فراگیر یا پوششی را تشکیل میدهند.
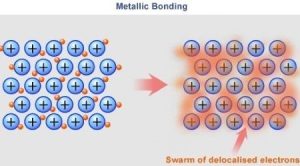
شکل 4: تشکیل پیوند فلزی
خواص فلزات
وجود پیوندهای فلزی عامل مهمی است که به فلزات خواص ویژه و منحصر به فردی میدهد. فلزات به روشهای خاصی رفتار میکنند و دارای ظاهری معمولی هستند. برخی از ویژگیهای پیوندهای فلزی عبارتند از: استحکام، چکش خواری، شکل پذیری، هدایت حرارتی و الکتریکی و…
نتیجه گیری
در این مقاله، پیوندهای یونی و کووالانسی را معرفی کردیم. سپس به توضیح پیوند فلزی و نحوه تشکیل آن پرداختیم. در این مقاله آموختیم که الکترونها بین بسیاری از اتمهای عنصر فلزی به اشتراک گذاشته می شود و این باعث میشود تا فلز خواص منحصر به فرد خود را بیابد.
